현재의 유럽 체외진단용 의료기기 지침 제 98/79/ EC 호 IVDD) 에 기반한 C E 인증서는 오는 20 22 년 5 월 25일 까지 유효하며 , 2022 년 5 월 26 일부터는 유럽 체외진단용 의료기기 규정 제 2 017/746 호 IVDR) 로 대체되어 새로운 프로세스의 적용이 시작됩니다.
본 과정을 통해 유럽 IVD 규정에 따른 기술문서 작성의 요구사항을 학습 할 수 있으며 IVD 제품을 서포트하기 위한 문서 작성과 검토를 할 수 있습니다.
▒교육대상
제품인증 / 품질 담당부서장
▒세부사항
- 교육일정
2일(16시간), 비합숙
- 교육비용
65만원 (면세, 교재, 중식 제공)
- 교육장소
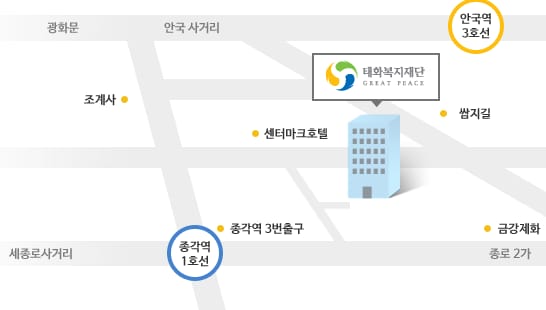
서울시 종로구 인사동 5길 29 태화빌딩 8층 BSI Training Center (03162)
(지하철 1호선 종각역 3번출구 도보 3분)
▒교육일정
