Quali dispositivi medici rientrano nella categoria “generali”?
BSI Medical Devices ha un team di technical specialists con esperienza in tutti i tipi di dispositivi medici. Questi sono solo alcuni dei dispositivi su cui il nostro team General offre supporto:
Dispositivi medici impiantati
Dispositivi di riparazione della parete addominale e dell'ernia, impianti gastrointestinali, impianti neurologici, impianti ricostruttivi dei tessuti molli, impianti renali, microsfere di embolizzazione, agenti emostatici e adesivi per tessuti
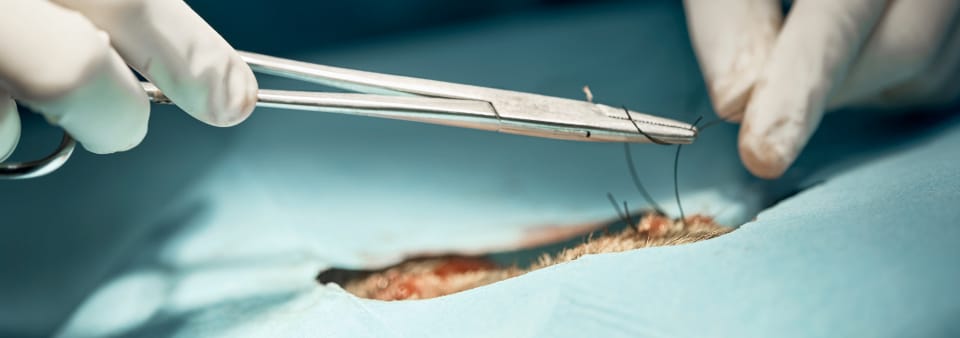
Dispositivi medici per la cura delle ferite e della cute
Bende, creme e gel barriera, suture e morsetti, soluzioni per la pulizia delle ferite, medicazioni avanzate, dispositivi per interventi chirurgici
Dispositivi medici oftalmici
Soluzioni per lenti a contatto, lenti a contatto, lenti intraoculari, dispositivi diagnostici oftalmici, dispositivi prostetici oftalmici, stent oftalmici, strumenti chirurgici oftalmici
Dispositivi medici per infusione e trasfusione
Sacche di sangue, tubi per il sangue, soluzioni, concentrati, polveri e dialisati per dialisi, set per infusione, set per trasfusione
Altri dispositivi medici
Dispositivi per anestesia, emergenza e terapia intensiva, soluzioni disinfettanti, strumentazione chirurgica generale, guanti, dispositivi ingeribili, preservativi e lubrificanti, dispositivi intrauterini, dispositivi che utilizzano nanomateriali, dispositivi per la somministrazione, la canalizzazione e la rimozione di sostanze
Dispositivi ai sensi di Annex XVI MDR
Dispositivi privi di finalità mediche previste di cui al Regolamento (UE) 2017/745 articolo 1, paragrafo 2. I dispositivi includono lenti a contatto o altri articoli destinati a essere introdotti nell'occhio o sull'occhio; impianti allo scopo di modificare l'anatomia o fissare parti del corpo come le protesi mammarie (esclusi i prodotti per tatuaggi e i piercing), sostanze destinate al riempimento del viso o di altre membrane dermiche/mucose come i filler dermici (esclusi i prodotti per tatuaggi); attrezzature per la liposuzione, la lipolisi o la lipoplastica.
Nei casi in cui i prodotti richiedano ulteriori competenze, collaboriamo con i nostri medici interni e con altri team tecnici.